曾被视为惰性的PVP,
竟然粘上了生物膜?
PVP adheres to the biofilm
参考文献
Crow, B., Stokes, W. E., Kapur, N., Busquets Fite, M., & Nelson, A. (2024).
Polyvinylpyrrolidone (PVP) adsorbs on and.interacts.with.biomembrane-like layers.Journal..of..Solid State Electrochemistry,28,411–418
https://doi.org/10.1007/s10008-023-05784-4
01
PVP
BIOMEMBEANE
PVP惰性还是亲和?
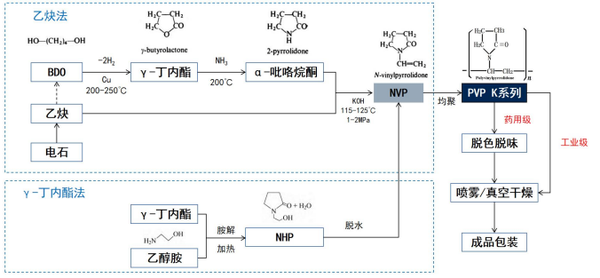
聚乙烯吡咯烷酮(PVP)是一种应用广泛的高分子材料。由于它不带电荷(非离子型)、化学性质稳定,对生物体和材料缺乏活性 ,一直被视作“惰性”的存在。举个例子, PVP常被用作纳米材料分散的稳定剂 —它可以吸附并包覆在纳米粒子表面,形成一层中性的“外衣”,防止颗粒相互聚集。在医药领域,许多纳米药物载体都会涂上一层PVP,借助其良好的生物相容性和惰性来提高稳定性。然而,PVP真的像我们以为的那样对生物膜毫无感觉吗?
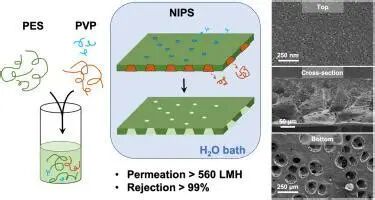
其实早有线索表明,PVP并非完全不互动的“路人”。它由许多N-乙烯基吡咯烷酮单体串联而成,每个单体上只有一个可供氢键结合的受体(羰基),亲油性也很低(log P值只有0.37)。这意味着单个PVP片段本身偏好留在水中,不太“喜欢”钻进脂质膜的油性区域。但当这些不起眼的亲水小单元连接成长链,会不会产生意想不到的“黏性”呢?2024年发表在《固态电化学杂志》上的一项研究专门探讨了这个问题。正如其标题所示:“PVP会吸附在类生物膜上并与之相互作用”。这一发现引发了关于PVP究竟“惰性”还是对生物膜有亲和力的有趣讨论。下面,我们就通过通俗的类比和实验解析,一探这段PVP“粘上”生物膜的故事。
02
PVP
BIOMEMBEANE
PVP粘上生物膜的故事
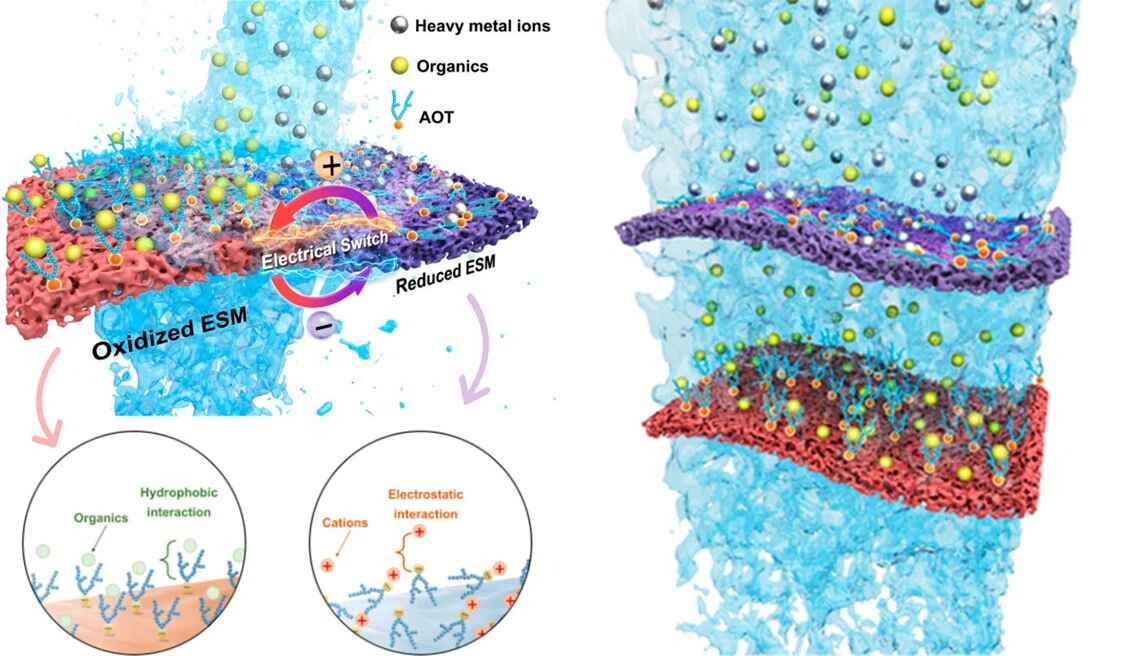
想象一下,细胞膜好比一层表面带点儿水分的“双面胶”,外侧是亲水的极性头部,内侧是疏水的脂肪尾部。而PVP呢,则像一条在水中游荡的长丝带:它本性亲水,不爱沾油,就像丝带喜欢飘在水里,不愿贴在油腻腻的表面。但事情没有那么简单。当一条足够长的丝带经过细胞膜附近时,情况可能发生变化:丝带的一些段落或许会被膜表面的极性“胶面”轻轻粘住。起初,只是一两个点黏上了(毕竟每段PVP链只能提供一个“小吸盘”去吸引极性头部)。如果丝带很短,可能粘不牢,很快又漂走了。但假如丝带很长,很长—长到可以在膜表面反复缠绕、打几个圈,那么靠着多个点的微弱吸附叠加,它反而可能挂在那层膜上不走了!
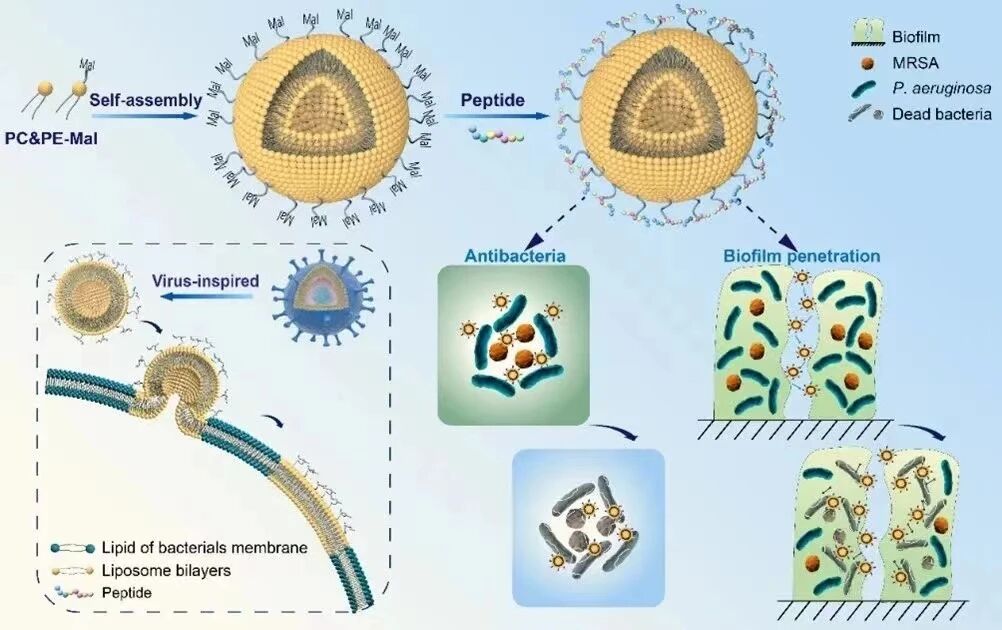
这个过程有点像八爪鱼抱石头。短的小触手吸附力有限,抱不住光滑的岩石;可一旦触手又多又长,能同时攀附多个支点,还能绕一圈“锁住”岩石,那八爪鱼就稳稳贴在上面了。同理,长链的PVP分子或许能以“多点黏附+自身盘绕”的方式,牢牢附着在生物膜表面,而不再像短链那样说来就来、说走就走。于是,一个原本被视作“不粘人”的高分子,开始表现出令人惊讶的“粘人”特质
03
PVP
BIOMEMBEANE
实验揭秘: PVP是如何贴上生物膜的?
实验设计
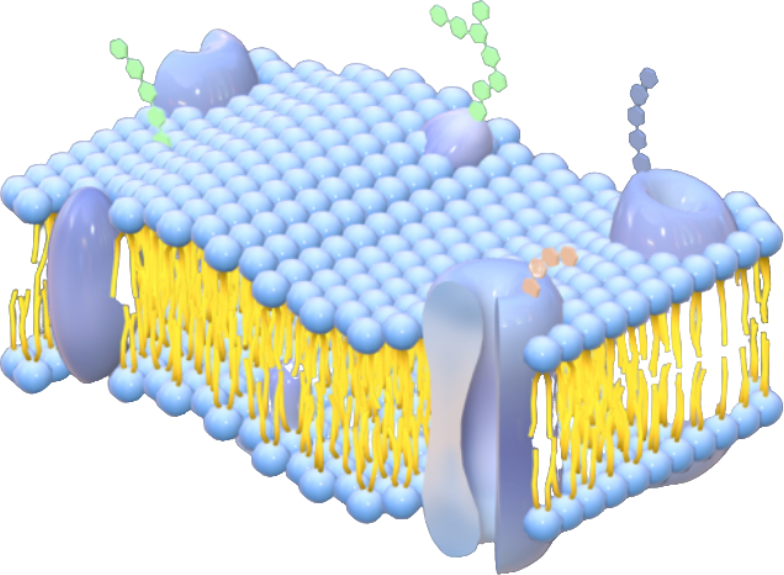
科学家们并非凭空想象这段“粘人”故事,而是通过巧妙的实验直接观测到了PVP的这一亲和行为。那么,他们是怎么做到的呢?首先,需要准备一个模拟生物膜。研究中采用的是一层由二油酰基磷脂酰胆碱(DOPC)组成的磷脂单分子层,它被支撑在一个特殊电极上。DOPC是种典型的磷脂分子,带有亲水头和疏水尾,在水界面能自组装成类似细胞膜的一层。想象这层磷脂就像铺在电极表面的“一层细胞膜”。接下来,研究人员使用电化学手段来监测这层膜的状态,其中的核心技术叫做快速循环伏安法(RCV)。简单来说,就是让电极电压在一定范围内快速来回扫动,并记录通过膜的电流变化。
为什么要看电流呢?
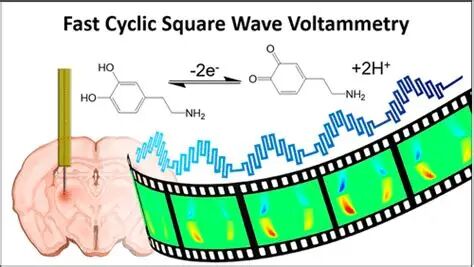
原来,当对磷脂膜施加电场时,会诱导膜发生结构变化,引起电流信号的波动。例如,在扫描电压过程中,这种磷脂单层膜会出现两个明显的电流峰,分别对应膜结构的特定变化:峰1表示电解质离子开始渗入磷脂层,峰2则对应单分子层重新排列成双层小斑块。可以把这两个尖锐的电流峰想象成膜在电场中“活动”的标志。膜要是受到干扰,这两个峰的形状和高度就会发生改变。因此,通过观察电流-电压曲线的峰形,我们就能侦测有没有东西在干扰膜。研究人员将不同链长的PVP溶液缓缓流过带膜电极,用RCV记录电流曲线,看看膜有没有响应变化。结果会如何呢?
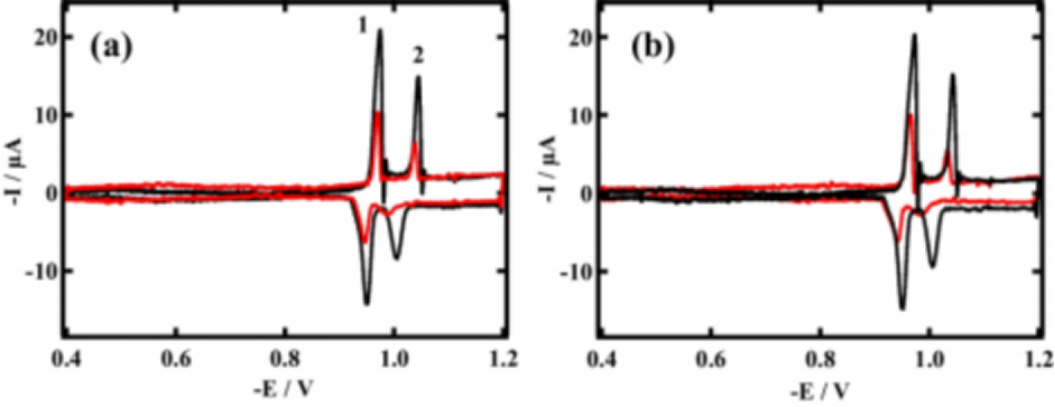
图2:快速循环伏安法(RCV)测得的磷脂单层膜电流 - 电压曲线(黑色)以及加入PVP后的变化(红色)示意图 。黑色曲线的尖峰1和2是未受干扰的膜在电场中产生的特征峰;加入PVP后(红线),可以看到峰值明显被压低。这种峰电流的抑制 就揭示了PVP在膜表面发生了吸附作用:仿佛在膜上按了 一层“垫子”,使原本锐利的信号变小。值得注意的是,红色曲线的基线并没有抬升,峰位也没有左右移动或变宽,这说明PVP只是停留在膜表面 ,并未深入膜的疏水内部或引发膜结构的大范围紊乱 。换言之,PVP就像附着在膜表面的一层薄薄涂层,削弱了膜对电场的响应,却没有撕裂或渗透进膜内层。
效果对比
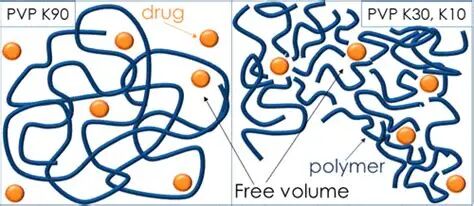
科学家进一步量化了不同分子量PVP的作用效果。他们比较了短链和长链PVP的表现:如果PVP与膜有亲和作用,那么随着溶液中PVP浓度增加,电流峰的抑制程度也会增加。不过增加的方式可能不同—是线性不断增加,还是逐渐趋于饱和?实验发现,这取决于PVP的链长。对于较短的PVP链(例如分子量3.5k和10k,对应约31和90个单体),峰值抑制百分比基本随浓度线性增长;而对于很长的PVP链(55k以上,对应数百上千单体),曲线呈现出典型的朗缪尔饱和形态:一开始抑制随浓度上升很快,但到一定浓度后趋于平台。这意味着长链PVP在膜表面铺满后,吸附效应就接近极限,继续加更多也压不下去了;相比之下,短链PVP因为个头小,要覆盖同样面积需要更多分子,所以在实验浓度范围内尚未达到饱和。
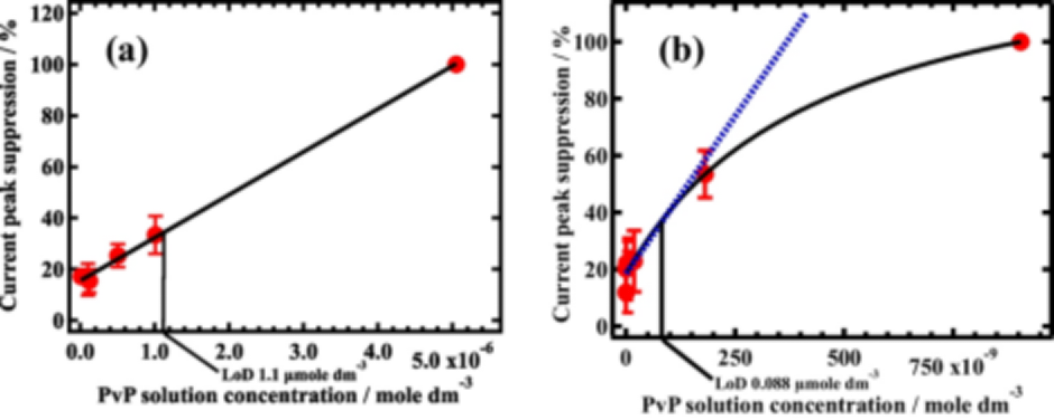
图3:PVP对磷脂膜电流峰抑制率随浓度变化的校准曲线对比。(a)短链PVP(约90单体)产生的峰抑制随着浓度近似线性增加,未显露出饱和值; (b) 长链PVP(约3239单体) 的曲线则呈现饱和弧线趋势,符合朗缪尔吸附模型 。横轴为溶液中PVP浓度,纵轴为电流峰抑制百分比。可以看出,长链PVP在极低浓度(纳摩尔级别)下就能引起显著的峰值压低且逐渐饱和,而短链PVP即使浓度提高到微摩尔级,曲线仍在接近线性地上升。
实验结果
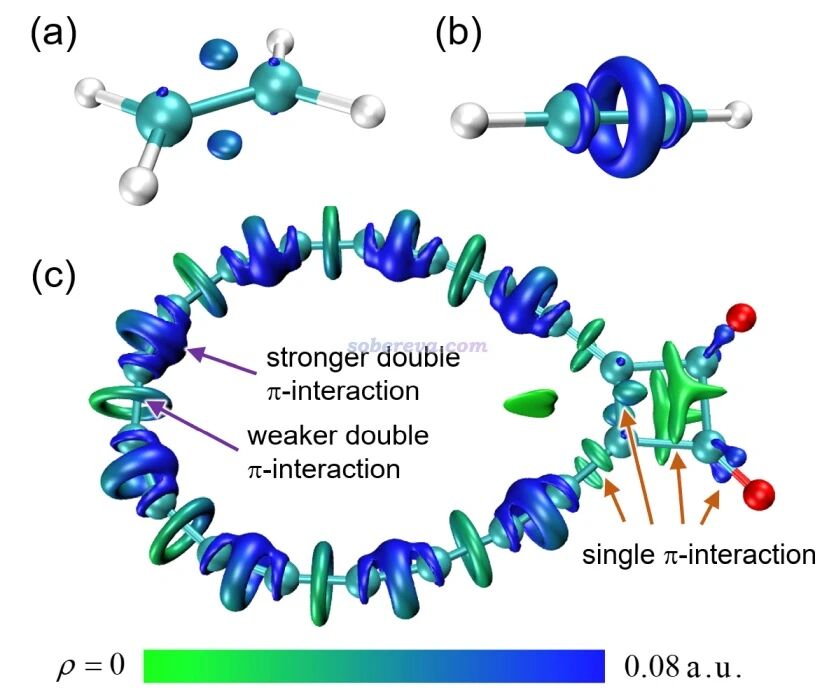
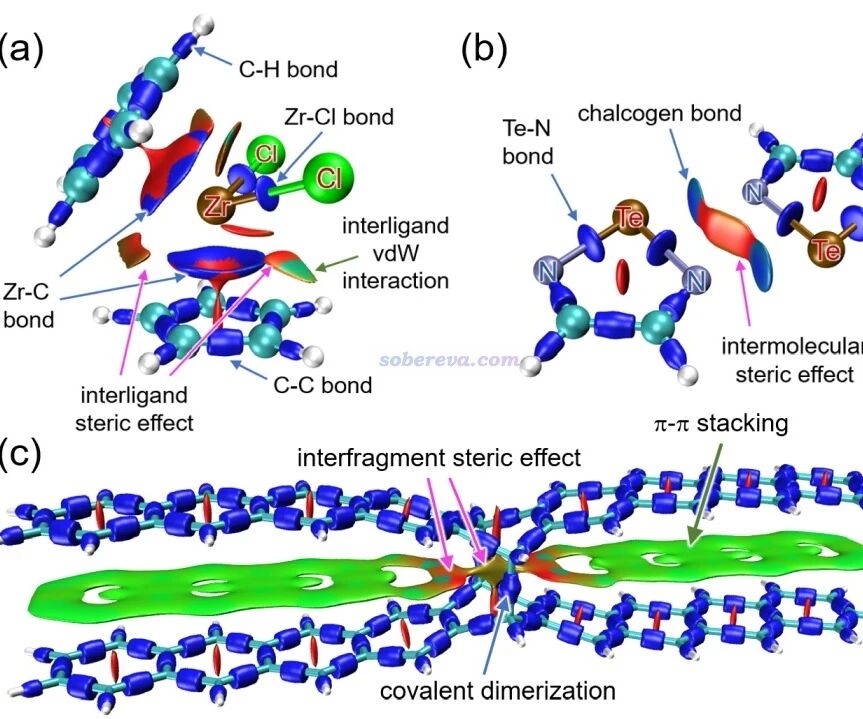
通过这样的比较,研究人员引入了“吸附亲和常数” (K<sub>2</sub>)和“检测限浓度”(LoD)等参数来表征 PVP对膜的亲和力强弱,并考察它们与聚合链长度的关系。结果表明, PVP链越长,其与膜的总体结合亲和力越大,但如果按每一个单体单位来平均计算,短链反而显得“更有效”一些。这听起来矛盾,其实暗示了吸附背后两种机制的存在:一方面,PVP吸附主要受熵驱动,也就是当聚合物贴上膜时,原本束缚在聚合物和膜表面的水分子被释放到溶液中,体系混乱度增加,提供了吸附的动力。短链PVP虽然与膜接触少,但每增加一个单体都能释放一点水,因而起初单位长度看来挺“有效”。但另一方面,随着链变长,另一个焓驱动因素开始起作用:长链PVP在膜表面可以发生链段间的非共价相互作用(比如链和链纠缠、聚集),这些额外的分子间“拉力”进一步促进了吸附。简单来说,短链主要是靠“赶走水”贴上去,而长链不仅赶走水,还会彼此抱团增粘,从而表现出更高的总亲和力。科研人员通过模型计算,将上述两种驱动力分别对应于一个指数项(随链长增长显著,加速上升)和一个幂律项(随链长增长渐缓)叠加,成功解释了实验数据。当然,这些深入的理论细节有兴趣不妨参考原论文,我们这里不再展开。
04
PVP
BIOMEMBEANE
从纳米药物到护肤品:发现有何意义?
研究动机
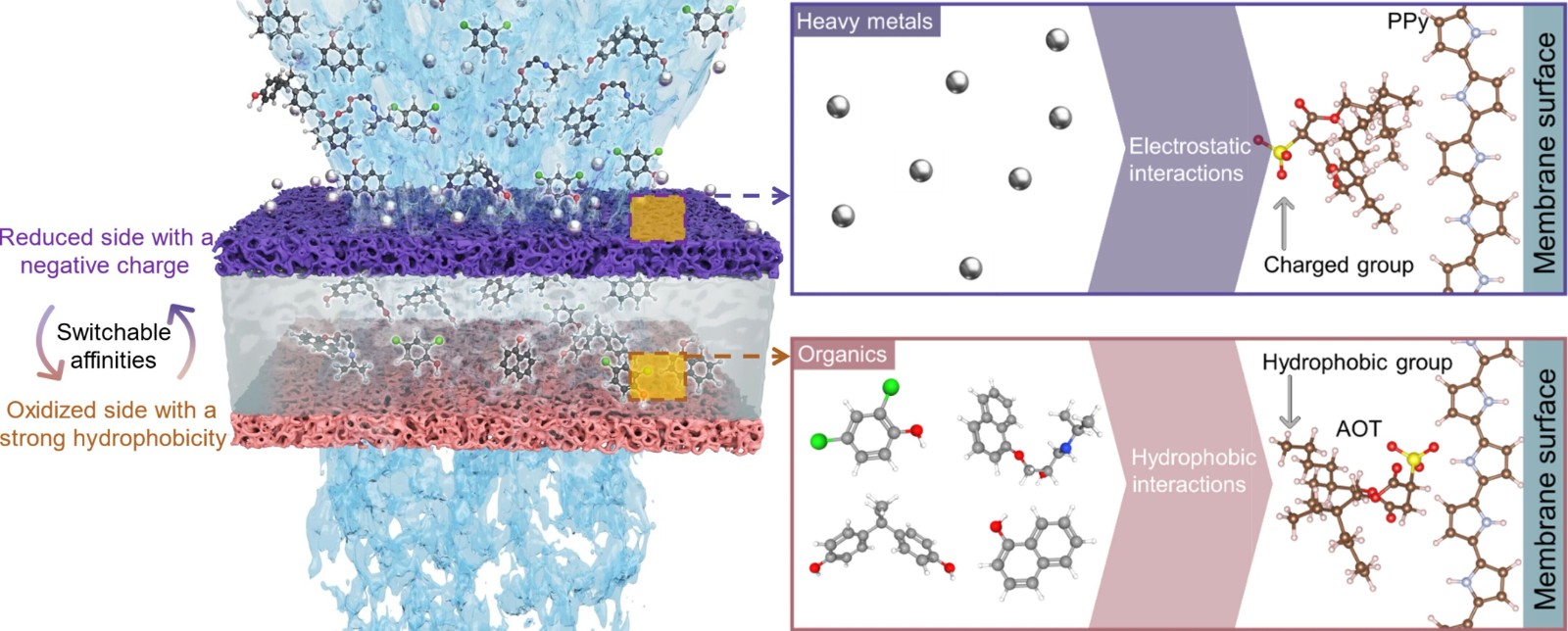
或许有人会问:一个实验发现PVP会黏附生物膜,这对我们的生活或技术有什么影响呢?其实影响可能比想象中大。首先,正如研究动机所指出的,由于大量纳米材料分散体都以PVP为涂层,我们有必要了解这层PVP对纳米材料与生物膜(如细胞膜)相互作用的影响。举个例子,银纳米颗粒常用PVP包覆来提高稳定性和生物相容性,用于抗菌敷料或药物载体。如果PVP链本身会黏附细胞膜,那PVP涂层就不只是被动的“保护衣”,而可能主动影响纳米粒子如何接近、黏附甚至进入细胞。它可能让纳米颗粒更容易附着在细胞膜上(因为PVP拉近了它们与膜的距离),也可能在颗粒表面形成一个“不黏滑垫”阻碍颗粒直接插入膜。具体效应如何,需要进一步实验评估。但显而易见的是,我们不能再想当然地把PVP视作完全惰性的背景材料,而应将其视为纳米系统中一个可能的活跃参与者。
实际应用

其次,PVP在日常生活用品中也相当常见。例如,在化妆品和护肤品中,PVP经常充当成膜剂或增稠剂,用于发胶、定型喷雾以及保湿护肤品等。下次你翻看护肤品成分表,看到“聚乙烯吡咯烷酮”或者它的缩写PVP,别惊讶,这就是我们的主角。人们添加PVP,是利用它在皮肤表面形成透明薄膜、锁住水分的特性。然而,这层 PVP薄膜会不会与皮肤的角质层或细胞膜发生类似的吸附作用呢?我们的皮肤屏障由脂质双分子层组成,从成分上看与DOPC膜有相似之处。尽管护肤领域通常认为PVP对皮肤无刺激、无毒性(因此才被广泛采用),但这项研究提醒我们:PVP并非“完全隐形”。它或许会温和地黏附在皮肤表面的脂质上,发挥粘合作用。这种作用也许是有益的—例如帮助在皮肤上形成稳定保湿的膜—但也可能带来我们尚未深入研究的影响(比如长时间使用后是否影响皮肤天然屏障的更新)。总之,在关注有效成分之余,科学家和工程师也应留意这些所谓惰性添加剂的微观行为。
05
PVP
BIOMEMBEANE
总结与思考
曾几何时,PVP被当作一个默默无闻的“背景板”材料:不参与反应,不干扰生物过程,只发挥物理作用。然而,上述研究让我们看到,即使是号称惰性的高分子,也会在特定情境下展现出亲和力和相互作用。PVP会吸附在模拟生物膜上,且链越长黏得越牢—这一结果发人深省。这不仅纠正了我们对PVP的认知偏差,也为材料科学和生物医学领域提供了新的思考方向:那些被反复使用的“惰性”材料,真的像想象中那样与世无争吗?也许在看不见的微观界面上,它们正发挥着被我们忽视的作用。正如物理学家费曼所言:“万物之底必有惊奇”。科学的有趣之处正在于此—越是看似平平无奇的东西,越可能隐藏不为人知的秘密。对PVP的再认识只是一个开始,展望未来,我们有理由去探索更多日常材料的“另一面”。当我们真正了解了手中所用之物的脾性,才能更加游刃有余地将它们用在刀刃上,或避免潜在的意外。你是否也开始好奇,还有哪些习以为常的材料,其实在悄悄地“粘”着这个世界?

|PVP业之先锋
|021-50565706


